Садржај
- Главна разлика
- Упоредни графикон
- Шта су јонска једињења?
- Шта су молекуларна једињења?
- Јонска једињења вс молекуларна једињења
Главна разлика
Једињење је препознато као супстанца која се формира када се два или више елемената комбинују у одређеним размерама кроз хемијску везу. Јонско једињење је једињење које настаје услед привлачења електростатичке силе између метала и неметала. Обично се јонска једињења појављују у распродатом кристалном стању. Поред тога, јонска једињења су добри проводници електричне енергије и имају високе тачке топљења и кључања. Са друге стране, молекуларна једињења настају услед дељења електрона између два не метала. У односу на јонска једињења, они су лоши проводници електричне енергије и имају ниску талиште и тачку кључања.
Упоредни графикон
| Јонска једињења | Молекуларна једињења | |
| Формација | Јонска једињења настају услед привлачења електростатичке силе између метала и неметала. | Молекуларна једињења настају захваљујући дељењу електрона између два неметала. |
| Група | Јонска једињења настају између метала и не-менталног. | Молекуларна једињења настају када се хемијски комбинују два неметала |
| Бонд | Јонско једињење настаје захваљујући електростатичкој привлачној сили познатој као јонска веза. | Молекуларна једињења настају због ковалентне везе између елемената. |
| Тачка топљења и кључања | Високо | Ниска |
| Држава | Јонска једињења су увек у чврстом стању, формирајући кристални изглед. | Молекуларна једињења могу бити у било ком стању, чврста, течна или гасна на собној температури. |
| Проводник електричне енергије | Добро | Лоше |
Шта су јонска једињења?
Ова једињења настају услед привлачења електростатичке силе између метала и неметала. Једноставнијим речима, сила (јонско везивање) у томе чини позитивно и негативно наелектрисано реакцију заједно да би направили једињење. Обично се јонска једињења појављују у распродатом кристалном стању и добри су проводници електричне енергије који имају високе тачке топљења и кључања. Јонска једињења настају између метала и неметала и имају неку врсту сјајног изгледа.
Пример: Столна сол (НаЦл) је најчешћи пример јонског једињења. У овој формацији натријум (НА) је метал, а хлор (Цл) је не метал, оба се држе заједно због електростатичке силе привлачења између њих обоје.
Шта су молекуларна једињења?
Једињења која настају дељењем електрона између неметала позната су као Молекуларно једињење. Елементи који овде реагују држе се заједно због ковалентне везе и зато се ова једињења често називају ковалентним једињењима.У односу на јонска једињења, они су лоши проводници електричне енергије и имају ниску талиште и тачку кључања.
Пример: У Озону (О3), кисеоник се комбинује са дељењем електрона да би формирао Озон.
Јонска једињења вс молекуларна једињења
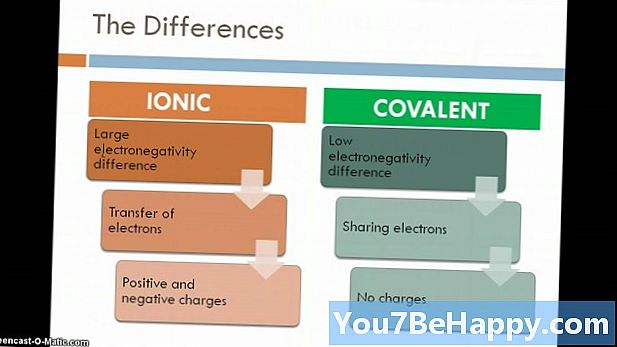
- Јонска једињења настају услед привлачења електростатичке силе између метала и неметала, док се молекуларна једињења формирају услед дељења електрона између два неметала.
- Молекуларна једињења настају када се два не метала хемијски комбинују, са друге стране јонска једињења настају између метала и не-менталних.
- Молекуларна једињења настају услед ковалентне везе између елемената, док се јонско једињење ствара услед електростатичке силе привлачења познате као јонска веза.
- Молекуларна једињења имају ниску талиште и тачку кључања у поређењу са јонским једињењима.
- Молекуларна једињења могу бити у било ком стању, чврста, течна или гасна на собној температури, док су јонска једињења увек у чврстом стању и формирају кристални изглед.
- Молекуларна једињења су слаб проводник електричне енергије, док су јонска једињења добар проводник електричне енергије.


